Contoh Soal Menentukan hasil kali kelarutan
Contoh Soal Menentukan hasil kali kelarutan - Dalam topik ini, kita akan membahas tentang penentuan hasil kali kelarutan (Ksp). Pada topik sebelumnya, kalian pasti telah mempelajari tentang kelarutan garam dalam air.
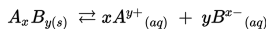
Nilai hasil kali kelarutannya dinyatakan dengan rumus berikut.
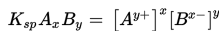

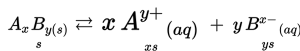
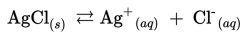
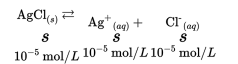
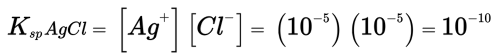
Mari kita ingat kembali topik yang telah lalu tersebut untuk memudahkan kita dalam mempelajari topik ini. Kelarutan garam dalam air berbeda-beda. Ada yang mudah larut dalam air dan ada juga yang sukar larut dalam air. Contoh garam yang mudah larut dalam air adalah natrium klorida (NaCl), sedangkan contoh garam yang sukar larut dalam air adalah perak klorida (AgCl). Kelarutan digunakan untuk menyatakan jumlah maksimum suatu zat yang dapat larut di dalam suatu pelarut. Besarnya kelarutan dipengaruhi oleh jenis pelarut, jenis zat terlarut, dan suhu.
Baiklah, tentu kalian telah ingat kembali hal-hal yang perlu kalian pahami sebagai modal dasar dalam mempelajari topik ini, yaitu menentukan hasil kali kelarutan.
Baiklah, tentu kalian telah ingat kembali hal-hal yang perlu kalian pahami sebagai modal dasar dalam mempelajari topik ini, yaitu menentukan hasil kali kelarutan.
1. Pengertian Hasil Kali Kelarutan (Ksp)
Perak klorida (AgCl) merupakan salah satu contoh garam yang sukar larut dalam air. Jika kita melarutkan AgCl ke dalam air, ternyata hanya sedikit garam AgCl yang larut. Sebagian besar garam AgCl tersebut tidak larut dan mengendap di dasar gelas. Larutan AgCl merupakan larutan yang mudah jenuh. Setelah larutan mencapai keadaan jenuh ternyata proses melarut dari garam tersebut tidak berhenti. Pada larutan jenuh tersebut tetap terjadi proses melarut, tetapi pada saat yang sama terjadi pula proses pengkristalan dengan laju yang sama. Pada saat keadaan jenuh tersebut terdapat kesetimbangan antara zat padat tak larut dengan ion-ionnya. Tetapan kesetimbangan dari kesetimbangan antara garam atau basa yang sedikit larut disebut tetapan hasil kali kelarutan (Ksp).
2. Penentuan Hasil Kali Kelarutan
Pada larutan jenuh, senyawa AxBy di dalam air akan menghasilkan reaksi kesetimbangan.
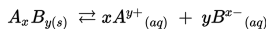
Nilai hasil kali kelarutannya dinyatakan dengan rumus berikut.
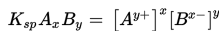
Langkah-langkah menentukan hasil kali kelarutan
1. Membuat reaksi kesetimbangan larutan jenuh senyawa AxBy dalam air.

2. Menentukan hubungan antara konsentrasi ion-ion dengan kelarutan berdasarkan koefisien reaksinya.
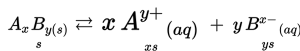
3. Mensubstitusi nilai konsentrasi ion-ion di atas ke dalam rumus hasil kali kelarutan.
Contoh Soal:
Kelarutan AgCl dalam air sama dengan 10-5 mol / L. Tentukan nilai Ksp AgCl!
Penyelesaian:
Mari kita perhatikan langkah-langkah dalam penentuan hasil kali kelarutan.
1. Membuat reaksi kesetimbangan larutan jenuh AgCl dalam air.
Penyelesaian:
Mari kita perhatikan langkah-langkah dalam penentuan hasil kali kelarutan.
1. Membuat reaksi kesetimbangan larutan jenuh AgCl dalam air.
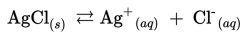
2. Menentukan hubungan konsentrasi ion-ion dengan kelarutan berdasarkan koefisien reaksinya.
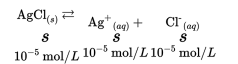
3. Mensubstitusi nilai konsentrasi ion-ion di atas ke dalam rumus hasil kali kelarutan.
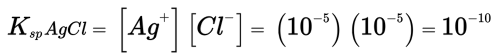
S1
Jika kelarutan PbI2 dalam air sama dengan s mol / L, maka nilai Ksp bagi garam ini adalah….
S2
Kelarutan CaF2 dalam air murni adalah 0,02 mol / L. Hasil kali kelarutan CaF2 adalah….
S3
Kelarutan Ca(OH)2 (Mr = 74) dalam 200 mL air adalah 0,322 gram. Hasil kali kelarutan Ca(OH)2 adalah.…
S4
Larutan jenuh X(OH)2 mempunyai pH = 10. Hasil kali kelarutan (Ksp) dari X(OH)2 adalah.…
S5
Suatu larutan jenuh X(OH)2 mempunyai kelarutan dalam air sebesar 5 x 10-6 mol/L. pH larutan jenuh tersebut adalah….
S6
Jika Ksp Ag2C2O4 adalah 32a3, maka kelarutan garam tersebut dalam air adalah….
S7
Contoh garam yang sukar larut dalam air adalah.…
S8
Pada suhu tertentu, 0,70 gram BaF2 ( Mr = 175) larut dalam air murni membentuk 2 L larutan jenuh. Hasil kali kelarutan larutan BaF2 adalah….
S9
Rumus hasilkali kelarutan (Ksp) untuk senyawa Ag2S adalah….
S10
Larutan jenuh suatu hidroksida X(OH)3 mempunyai pH = 9. Harga Ksp dari X(OH)3 adalah….
