Contoh Soal Sifat-Sifat Logam Alkali
Contoh Soal Sifat-Sifat Logam Alkali - Pada topik sebelumnya, kalian telah mempelajari tentang kelimpahan unsur-unsur di alam. Pada topik ini, kalian akan belajar tentang sifat-sifat logam alkali. Seperti apa sifat-sifat logam alkali? Untuk memahami hal tersebut, perhatikan analogi berikut ini.
Pernahkah kalian memperhatikan sifat-sifat anggota keluarga kalian? Meskipun memiliki sifat-sifat yang berbeda, namun pasti ada kemiripan sifat antara satu dengan yang lain. Contohnya keluarga Adi yang terdiri dari ayah, ibu, dan 6 orang anak. Mereka menempati komplek perumahan blok S. Anaknya bernama Litia, Natria, Kalina, Rudi, Sesilia, dan Frans. Litia, Natria, dan Sesilia memiliki sifat yang sama yaitu pemalu dan pendiam. Sementara Kalina, Rudi, dan Frans memiliki sifat pemberani dan mudah bergaul. Bentuk fisik anak-anak perempuan mengikuti ibunya, yaitu ramping, rambut ikal, mata sipit, dan kulit kuning langsat. Sementara bentuk fisik anak laki-laki mengikuti ayahnya, yaitu agak gemuk, mata bulat, rambut lurus, dan kulit sawo matang. Begitu juga dengan logam alkali. Masing-masing unsur alkali memiliki kemiripan sifat antara satu dengan yang lain.
Bagaimanakah sifat-sifat logam alkali? Untuk memahami hal tersebut, mari kita simak ulasan berikut.
☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳
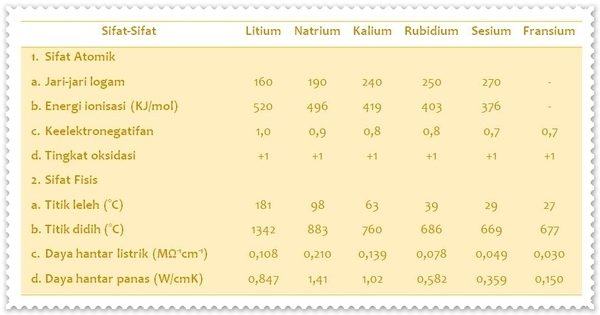
Unsur-unsur alkali terdiri dari logam litium (Li), natrium (Na), kalium (K), rubidium, sesium (Cs), dan Fransium (Fr). Unsur logam alkali dalam tabel periodik terdapat pada golongan I A. Unsur alkali tergolong logam yang mempunyai sifat: merupakan konduktor listrik dan panas yang baik, permukaan mengkilap, dan mudah ditempa. Unsur-unsur alkali mudah melepas elektron valensinya membentuk ion-ion bermuatan +1. Untuk memahami kemiripan sifat-sifat unsur logam alkali, perhatikan data tabel berikut ini.
Bagaimanakah sifat-sifat logam alkali? Untuk memahami hal tersebut, mari kita simak ulasan berikut.
☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳
Unsur-unsur alkali terdiri dari logam litium (Li), natrium (Na), kalium (K), rubidium, sesium (Cs), dan Fransium (Fr). Unsur logam alkali dalam tabel periodik terdapat pada golongan I A. Unsur alkali tergolong logam yang mempunyai sifat: merupakan konduktor listrik dan panas yang baik, permukaan mengkilap, dan mudah ditempa. Unsur-unsur alkali mudah melepas elektron valensinya membentuk ion-ion bermuatan +1. Untuk memahami kemiripan sifat-sifat unsur logam alkali, perhatikan data tabel berikut ini.

A. Sifat atomik unsur alkali ▩▩▩▩
1. Jari-jari atom
Jari-jari atom dalam satu golongan, dari litium sampai fransium semakin bertambah karena jumlah kulit elektronnya juga semakin bertambah.
2. Energi ionisasi
Energi ionisasi dalam satu golongan, dari litium sampai fransium semakin berkurang. Hal ini terjadi karena pertambahan jari-jari atom menyebabkan gaya tarik menarik inti dengan elektron valensi menjadi semakin lemah sehingga untuk melepas elektron dibutuhkan energi yang semakin kecil.
3. Keelektronegatifan
Keelektronegatifan dalam satu golongan, dari litium sampai fransium semakin berkurang. Hal ini berarti penurunan kemampuan atom dari litium sampai fransium untuk menarik elektron dari atom lain dalam pembentukan ikatan kimia.
4. Tingkat oksidasi
Tingkat oksidasi logam-logam alkali hanya satu macam yaitu +1. Hal ini menunjukkan bahwa untuk mencapai konfigurasi elektron stabil seperti gas mulia, logam-logam alkali melepas satu elektronnya.
Jari-jari atom dalam satu golongan, dari litium sampai fransium semakin bertambah karena jumlah kulit elektronnya juga semakin bertambah.
2. Energi ionisasi
Energi ionisasi dalam satu golongan, dari litium sampai fransium semakin berkurang. Hal ini terjadi karena pertambahan jari-jari atom menyebabkan gaya tarik menarik inti dengan elektron valensi menjadi semakin lemah sehingga untuk melepas elektron dibutuhkan energi yang semakin kecil.
3. Keelektronegatifan
Keelektronegatifan dalam satu golongan, dari litium sampai fransium semakin berkurang. Hal ini berarti penurunan kemampuan atom dari litium sampai fransium untuk menarik elektron dari atom lain dalam pembentukan ikatan kimia.
4. Tingkat oksidasi
Tingkat oksidasi logam-logam alkali hanya satu macam yaitu +1. Hal ini menunjukkan bahwa untuk mencapai konfigurasi elektron stabil seperti gas mulia, logam-logam alkali melepas satu elektronnya.
B. Sifat fisis unsur alkali ▩▩▩▩
1. Titik leleh dan titik didih
Titik leleh dan titik didih dalam satu golongan, dari litium sampai fransium semakin berkurang. Hal ini disebabkan karena titik leleh dan titik didih ditentukan oleh jenis ikatan dan kekuatan ikatan logam yang dimiliki unsur alkali. Semakin kuat ikatan logamnya, semakin tinggi titik leleh dan titik didihnya.
2. Daya hantar listrik dan panas
Daya hantar listrik dan panas dalam satu golongan, dari litium sampai fransium semakin berkurang, kecuali pada logam natrium dan kalium yang semakin bertambah karena elektron valensi pada atom Na dan K mudah bergerak bebas.
Titik leleh dan titik didih dalam satu golongan, dari litium sampai fransium semakin berkurang. Hal ini disebabkan karena titik leleh dan titik didih ditentukan oleh jenis ikatan dan kekuatan ikatan logam yang dimiliki unsur alkali. Semakin kuat ikatan logamnya, semakin tinggi titik leleh dan titik didihnya.
2. Daya hantar listrik dan panas
Daya hantar listrik dan panas dalam satu golongan, dari litium sampai fransium semakin berkurang, kecuali pada logam natrium dan kalium yang semakin bertambah karena elektron valensi pada atom Na dan K mudah bergerak bebas.
C. Sifat kimia unsur alkali ▩▩▩▩
1. Kereaktifan
Unsur alkali termasuk logam yang sangat reaktif sehingga unsur ini cenderung lebih mudah melepas elektronnya. Kereaktifan logam alkali tampak dari kemudahannya bereaksi dengan air, unsur-unsur halogen, hidrogen, oksigen, dan belerang. Unsur logam alkali yang paling reaktif adalah sesium, sedangkan yang kurang reaktif adalah litium. Oleh karena itu, kereaktifan logam alkali dari atas ke bawah dalam sistem periodik semakin bertambah.
2. Sifat logam dan basa alkali
Logam alkali dapat bereaksi dengan air membentuk basa kuat. Dalam satu golongan, dari atas ke bawah, sifat basa logam alkali semakin kuat. Dari atas ke bawah, sifat logamnya juga semakin kuat. Basa senyawa alkali sangat mudah larut dalam air dan bersifat ionik.
3. Warna nyala
Logam alkali jika dibakar akan memberikan warna nyala yang khas.

Unsur alkali termasuk logam yang sangat reaktif sehingga unsur ini cenderung lebih mudah melepas elektronnya. Kereaktifan logam alkali tampak dari kemudahannya bereaksi dengan air, unsur-unsur halogen, hidrogen, oksigen, dan belerang. Unsur logam alkali yang paling reaktif adalah sesium, sedangkan yang kurang reaktif adalah litium. Oleh karena itu, kereaktifan logam alkali dari atas ke bawah dalam sistem periodik semakin bertambah.
2. Sifat logam dan basa alkali
Logam alkali dapat bereaksi dengan air membentuk basa kuat. Dalam satu golongan, dari atas ke bawah, sifat basa logam alkali semakin kuat. Dari atas ke bawah, sifat logamnya juga semakin kuat. Basa senyawa alkali sangat mudah larut dalam air dan bersifat ionik.
3. Warna nyala
Logam alkali jika dibakar akan memberikan warna nyala yang khas.

S1
Berikut ini merupakan sifat unsur alkali sebagai logam, kecuali ....
S2
Unsur logam alkali yang kurang reaktif terhadap air adalah ....
S3
Unsur logam alkali yang mempunyai warna nyala kuning adalah ....
S4
Energi ionisasi unsur alkali secara acak adalah 496 KJ/mol; 403 KJ/mol; 419 KJ/mol; 376 KJ/mol; dan 520 KJ/mol. Energi ionisasi dari litium adalah ... KJ/mol.
S5
Unsur alkali yang mempunyai titik didih terbesar adalah ....
S6
Keelektronegatifan unsur-unsur alkali secara acak adalah 0,7; 0,8; 1,0; 0,7; 0,8; 0,9. Keelektronegatifan dari natrium adalah ....
S7
Unsur logam alkali yang mempunyai warna nyala biru adalah ....
S8
Titik leleh unsur kalium adalah ....
S9
Tingkat oksidasi unsur logam alkali adalah ....
S10
Manfaat dari senyawa natrium benzoat adalah ....
