Contoh Soal Sifat-Sifat Logam Alkali Tanah
Contoh Soal Sifat-Sifat Logam Alkali Tanah - Unsur-unsur logam alkali tanah meliputi berilium (Be), magnesium (Mg), kalsium (Ca), Stronsium (Sr), Barium (Ba), dan Radium (Ra). Logam-logam tersebut terletak pada golongan II A pada sistem periodik unsur. Penamaan alkali tanah dikarenakan pada umumnya unsur alkali ditemukan dalam tanah berupa mineral batuan.
1. Sifat-sifat fisis logam alkali tanah ❍❍❍❍

1. Sifat-sifat fisis logam alkali tanah ❍❍❍❍
Unsur-unsur logam alkali tanah pada umumnya berwarna perak, mempunyai kilat logam, relatif lunak, kecuali berilium yang agak keras. Selain berilium, logam alkali tanah dapat menghantarkan panas dan listrik dengan baik. Unsur-unsur alkali tanah mudah melepaskan elektron valensinya, membentuk ion-ion bermuatan +2. Untuk memahami kemiripan sifat-sifat unsur logam alkali tanah, perhatikan data tabel berikut ini.
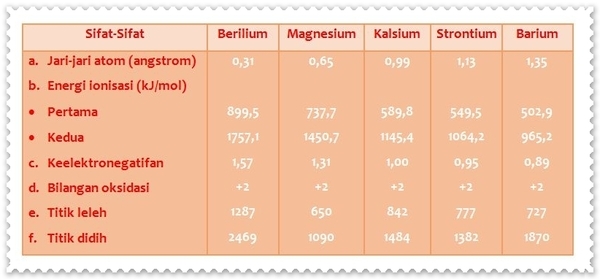
a. Jari-jari atom
Jari-jari atom dalam satu golongan dari berilium sampai barium semakin bertambah karena jumlah kulit elektronnya juga semakin bertambah. Jari-jari atomnya lebih kecil dan muatan intinya lebih besar sehingga logam alkali tanah lebih keras dibandingkan logam alkali.
b. Energi ionisasi
Energi ionisasi dalam satu golongan dari berilium sampai barium semakin berkurang. Hal ini terjadi karena pertambahan jari-jari atom menyebabkan gaya tarik menarik inti dengan elektron valensi menjadi semakin lemah sehingga untuk melepas elektron dibutuhkan energi yang semakin kecil.
c. Keelektronegatifan
Keelektronegatifan dalam satu golongan dari berilium sampai barium semakin berkurang. Hal ini berarti penurunan kemampuan atom dari berilium sampai barium untuk menarik elektron dari atom lain dalam pembentukan ikatan kimia.
d. Bilangan oksidasi
Bilangan oksidasi logam-logam alkali tanah hanya satu macam yaitu +2,yang menunjukkan bahwa untuk mencapai konfigurasi elektron stabil seperti gas mulia, logam-logam alkali tanah melepas dua elektronnya.
e. Titik leleh dan titik didih
Titik leleh dan titik didih logam alkali tanah tidak mempunyai keteraturan seperti sifat periodik yang lain. Namun pada umumnya, cenderung menurun dari berilium hingga barium.
2. Sifat-sifat kimia logam alkali tanah ❍❍❍❍
a. Jari-jari atom
Jari-jari atom dalam satu golongan dari berilium sampai barium semakin bertambah karena jumlah kulit elektronnya juga semakin bertambah. Jari-jari atomnya lebih kecil dan muatan intinya lebih besar sehingga logam alkali tanah lebih keras dibandingkan logam alkali.
b. Energi ionisasi
Energi ionisasi dalam satu golongan dari berilium sampai barium semakin berkurang. Hal ini terjadi karena pertambahan jari-jari atom menyebabkan gaya tarik menarik inti dengan elektron valensi menjadi semakin lemah sehingga untuk melepas elektron dibutuhkan energi yang semakin kecil.
c. Keelektronegatifan
Keelektronegatifan dalam satu golongan dari berilium sampai barium semakin berkurang. Hal ini berarti penurunan kemampuan atom dari berilium sampai barium untuk menarik elektron dari atom lain dalam pembentukan ikatan kimia.
d. Bilangan oksidasi
Bilangan oksidasi logam-logam alkali tanah hanya satu macam yaitu +2,yang menunjukkan bahwa untuk mencapai konfigurasi elektron stabil seperti gas mulia, logam-logam alkali tanah melepas dua elektronnya.
e. Titik leleh dan titik didih
Titik leleh dan titik didih logam alkali tanah tidak mempunyai keteraturan seperti sifat periodik yang lain. Namun pada umumnya, cenderung menurun dari berilium hingga barium.
a. Sifat kimia logam alkali tanah mirip dengan logam alkali. Akan tetapi, logam alkali tanah kurang reaktif dibandingkan dengan logam alkali dalam satu periode. Hal ini dikarenakan jari-jari atom logam alkali tanah lebih kecil dan elektron valensinya lebih banyak.
b. Logam alkali tanah dapat bereaksi dengan air, kecuali berilium tidak bereaksi dan logam magnesium hanya bereaksi dengan air panas.
c. Semua logam alkali tanah bereaksi dengan asam kuat membentuk garam dan gas hidrogen. Jika berilium bereaksi dengan basa kuat akan menyebabkan sifat amfoter.
3. Warna nyala logam alkali tanah ❍❍❍❍b. Logam alkali tanah dapat bereaksi dengan air, kecuali berilium tidak bereaksi dan logam magnesium hanya bereaksi dengan air panas.
c. Semua logam alkali tanah bereaksi dengan asam kuat membentuk garam dan gas hidrogen. Jika berilium bereaksi dengan basa kuat akan menyebabkan sifat amfoter.

S1
Magnesium mempunyai nomor atom 12 dan nomor massa 24. Jumlah elektron pada ion magnesium adalah ....
S2
Keelektronegatifan unsur alkali tanah secara acak adalah 1,00; 0,95; 1,31; 0,89; 1,57. Keelektronegatifan dari magnesium adalah ....
S3
Tingkat oksidasi unsur logam alkali tanah adalah ..
S4
Unsur logam alkali tanah yang mempunyai jari-jari atom terkecil adalah ....
S5
Senyawa logam alkali tanah yang digunakan sebagai obat maag untuk menetralkan asam lambung adalah ....
S6
Berikut ini merupakan unsur-unsur logam alkali tanah, kecuali ....
S7
Unsur logam alkali tanah yang mempunyai energi ionisasi terbesar adalah ....
S8
Unsur logam alkali tanah yang terletak pada periode 4 adalah ....
S9
Unsur logam alkali tanah yang mempunyai titik didih terbesar adalah ....
S10
Unsur logam alkali tanah yang tidak dapat bereaksi dengan air adalah ....
