Contoh Soal Sifat-Sifat Halogen
Contoh Soal Sifat-Sifat Halogen - Pada topik sebelumnya, kalian telah mempelajari tentang kelimpahan unsur-unsur di alam. Pada topik ini, kalian akan belajar tentang sifat-sifat halogen. Seperti apa sifat-sifat halogen? Untuk memahami hal tersebut, perhatikan analogi berikut ini.
Pernahkah kalian memperhatikan ciri-ciri fisik dan perbedaan sifat-sifat dalam satu anggota keluarga? Keluarga Samara terdiri dari ayah, ibu, dan 5 orang anak. Masing-masing anak memiliki sifat yang berbeda, tetapi antara satu dengan yang lain memiliki kemiripan sifat. Anak pertama, Flora, memiliki sifat pendiam. Anak kedua, Clara memiliki sifat pendiam. Anak ketiga, Bram, memiliki sifat periang. Anak keempat, Ida memiliki sifat pemalu. Anak kelima, Astuti memiliki sifat pendiam. Kelima anak tersebut memiliki ciri fisik yang sama, yaitu hidung mancung, rambut lurus, mata sipit, dan kulit kuning langsat. Akan tetapi, Bram dan Ida memiliki postur tubuh yang gemuk, sedangkan Flora, Clara, dan Astuti mempunyai postur tubuh langsing. Begitu juga dengan unsur–unsur halogen. Anggota unsur-unsur halogen meskipun memiliki sifat yang berbeda, namun antara yang satu dengan yang lain memiliki kemiripan sifat.
☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳
Bagaimanakah sifat-sifat fisik halogen? Untuk memahami hal tersebut, mari kita simak ulasan berikut.
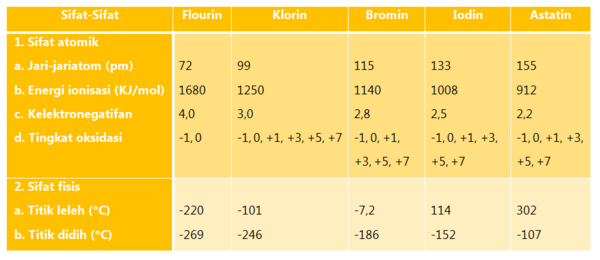
Unsur-unsur halogen terdiri dari flourin (F), klorin (Cl), bromin (Br), iodin (I), dan astatin (At). Unsur-unsur yang terletak pada golongan yang sama menunjukkan perubahan sifat secara beraturan. Perhatikan tabel berikut ini.
☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳☳
Bagaimanakah sifat-sifat fisik halogen? Untuk memahami hal tersebut, mari kita simak ulasan berikut.
Unsur-unsur halogen terdiri dari flourin (F), klorin (Cl), bromin (Br), iodin (I), dan astatin (At). Unsur-unsur yang terletak pada golongan yang sama menunjukkan perubahan sifat secara beraturan. Perhatikan tabel berikut ini.

A. Sifat Atomik Halogen ◉◉◉
1. Jari-Jari Atom
Jari-jari atom dalam satu golongan, dari flourin sampai astatin semakin bertambah karena jumlah kulit elektronnya juga semakin bertambah.
2. Energi Ionisasi
Energi Ionisasi dalam satu golongan, dari flourin sampai astatin semakin berkurang. Hal ini terjadi karena pertambahan jari-jari atom menyebabkan gaya tarik menarik antara inti dan elektron valensi menjadi semakin lemah sehingga untuk melepas elektron dibutuhkan energi yang semakin kecil.
3. Keelektronegatifan
Keelektronegatifan dalam satu golongan, dari flourin sampai astatin semakin berkurang. Hal ini berarti penurunan kemampuan atom dari flourin sampai astatin untuk menarik elektron dari atom lain dalam pembentukan ikatan kimia.
4. Tingkat Oksidasi
Pada umumnya, unsur-unsur halogen memiliki enam bilangan oksidasi, kecuali unsur fluorin yang hanya memiliki 2 bilangan oksidasi yaitu 0 dan -1.
Jari-jari atom dalam satu golongan, dari flourin sampai astatin semakin bertambah karena jumlah kulit elektronnya juga semakin bertambah.
2. Energi Ionisasi
Energi Ionisasi dalam satu golongan, dari flourin sampai astatin semakin berkurang. Hal ini terjadi karena pertambahan jari-jari atom menyebabkan gaya tarik menarik antara inti dan elektron valensi menjadi semakin lemah sehingga untuk melepas elektron dibutuhkan energi yang semakin kecil.
3. Keelektronegatifan
Keelektronegatifan dalam satu golongan, dari flourin sampai astatin semakin berkurang. Hal ini berarti penurunan kemampuan atom dari flourin sampai astatin untuk menarik elektron dari atom lain dalam pembentukan ikatan kimia.
4. Tingkat Oksidasi
Pada umumnya, unsur-unsur halogen memiliki enam bilangan oksidasi, kecuali unsur fluorin yang hanya memiliki 2 bilangan oksidasi yaitu 0 dan -1.
B. Sifat Fisis Halogen ◉◉◉
1. Wujud pada Suhu Ruangan
Flourin dan klorin mempunyai wujud gas, bromin mempunyai wujud cair, sedangkan iodin dan astatin berwujud padat.
2. Titik Leleh dan Titik Didih
Titik leleh dan titik didih dalam satu golongan, dari flourin sampai astatin semakin bertambah.
Flourin dan klorin mempunyai wujud gas, bromin mempunyai wujud cair, sedangkan iodin dan astatin berwujud padat.
2. Titik Leleh dan Titik Didih
Titik leleh dan titik didih dalam satu golongan, dari flourin sampai astatin semakin bertambah.
C. Sifat Kimia Halogen ◉◉◉
1. Kereaktifan
Pada umumnya, keberadaan halogen ditemukan di alam dalam bentuk senyawa. Hal ini menunjukkan bahwa unsur halogen merupakan unsur yang sangat reaktif. Keelektronegatifan mempengaruhi kereaktifan halogen. Semakin tinggi keelektronegatifan halogen, unsur halogen akan semakin reaktif. Hal ini disebabkan karena unsur halogen semakin mudah menarik elektron. Selain itu, kereaktifan halogen juga dipengaruhi oleh energi ikatan halogen. Jika ikatan tersebut mudah diputuskan, maka halogen bersifat reaktif.
2. Daya Oksidasi
Unsur-unsur halogen merupakan oksidator kuat. Sifat oksidator dalam satu golongan, dari flourin sampai astatin semakin berkurang. Hal ini menyebabkan unsur-unsur halogen dapat mengoksidasi ion halida di bawahnya. Sebaliknya, sifat reduktor ion halida dalam satu golongan, dari flourin sampai astatin semakin bertambah.
Pada umumnya, keberadaan halogen ditemukan di alam dalam bentuk senyawa. Hal ini menunjukkan bahwa unsur halogen merupakan unsur yang sangat reaktif. Keelektronegatifan mempengaruhi kereaktifan halogen. Semakin tinggi keelektronegatifan halogen, unsur halogen akan semakin reaktif. Hal ini disebabkan karena unsur halogen semakin mudah menarik elektron. Selain itu, kereaktifan halogen juga dipengaruhi oleh energi ikatan halogen. Jika ikatan tersebut mudah diputuskan, maka halogen bersifat reaktif.
2. Daya Oksidasi
Unsur-unsur halogen merupakan oksidator kuat. Sifat oksidator dalam satu golongan, dari flourin sampai astatin semakin berkurang. Hal ini menyebabkan unsur-unsur halogen dapat mengoksidasi ion halida di bawahnya. Sebaliknya, sifat reduktor ion halida dalam satu golongan, dari flourin sampai astatin semakin bertambah.
S1
Unsur-unsur halogen memiliki enam tingkat oksidasi, kecuali ....
S2
Unsur halogen yang memiliki titik didih terbesar adalah ....
S3
Bilangan oksidasi Cl dari senyawa KClO₄ adalah ....
S4
Perhatikan tabel berikut.
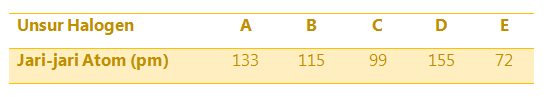
Urutan jari-jari atom halogen dalam satu golongan, dari atas ke bawah adalah ....

Urutan jari-jari atom halogen dalam satu golongan, dari atas ke bawah adalah ....
S5
Bilangan oksidasi I dalam NaIO₂ adalah ....
S6
Unsur halogen yang terletak pada golongan VII A periode 4 adalah ....
S7
Keelektronegatifan unsur-unsur halogen secara acak adalah 2,8; 3,0; 2,5; 4,0; 2,2. Keelektronegatifan dari iodin adalah ....
S8
Unsur halogen yang berwujud cair pada suhu ruangan adalah ....
S9
Unsur halogen yang berupa gas berwarna kuning kehijauan adalah ....
S10
Berikut ini merupakan senyawa halogen dengan unsur nonlogam, kecuali ....
