Contoh Soal Persamaan Gas Ideal
Contoh Soal Persamaan Gas Ideal - Dalam topik ini kita akan mempelajari sifat-sifat gas dalam ruang tertutup. Sekarang, mari kita pelajari satu per satu tentang definisi gas ideal, karakteristik, dan persamaan umum gas ideal.

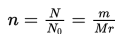
1.Definisi Gas Ideal
Karakteristik gas dalam ruang tertutup yang memenuhi kondisi-kondisi fisis tertentu disebut sebagai gas ideal. Gas ideal memiliki partikel yang mampu bergerak bebas ke segala arah, tumbukan partikel-partikelnya akan menghasilkan tumbukan lenting sempurna sehingga tidak terjadi kehilangan energi (loss energy). Gas ideal juga memiliki karakteristik yang spesifik terkait dengan tekanan P, volume V, dan suhu T.
2.Persamaan Umum Gas Ideal
Kondisi suatu gas ideal dapat dianalisa melalui tiga besaran fisis utama, yaitu tekanan (P), volume (V), dan suhu (T) dimana masing-masing besaran tersebut memiliki hubungan yang sangat spesifik. Hubungan ketiganya telah melahirkan rumusan-rumusan gas ideal sebagai berikut.
a.Hukum Boyle
Menyatakan bahwa pada suhu tetap tekanan gas akan berbanding terbalik dengan volumenya.
PV = Konstan
b.Hukum Gay-Lussac
Menyatakan bahwa pada tekanan tetap volume gas akan sebanding dengan suhunya.
Karakteristik gas dalam ruang tertutup yang memenuhi kondisi-kondisi fisis tertentu disebut sebagai gas ideal. Gas ideal memiliki partikel yang mampu bergerak bebas ke segala arah, tumbukan partikel-partikelnya akan menghasilkan tumbukan lenting sempurna sehingga tidak terjadi kehilangan energi (loss energy). Gas ideal juga memiliki karakteristik yang spesifik terkait dengan tekanan P, volume V, dan suhu T.
2.Persamaan Umum Gas Ideal
Kondisi suatu gas ideal dapat dianalisa melalui tiga besaran fisis utama, yaitu tekanan (P), volume (V), dan suhu (T) dimana masing-masing besaran tersebut memiliki hubungan yang sangat spesifik. Hubungan ketiganya telah melahirkan rumusan-rumusan gas ideal sebagai berikut.
a.Hukum Boyle
Menyatakan bahwa pada suhu tetap tekanan gas akan berbanding terbalik dengan volumenya.
PV = Konstan
b.Hukum Gay-Lussac
Menyatakan bahwa pada tekanan tetap volume gas akan sebanding dengan suhunya.

c. Persamaan Umum Gas Ideal
PV = nRT
n = jumlah mol
R= konstanta gas universal 8,314 J/mol K
PV = nRT
n = jumlah mol
R= konstanta gas universal 8,314 J/mol K
Untuk dapat menyelesaikan soal-soal persamaan gas ideal, kita perlu mengetahui tentang konsep mol. Dalam keadaan standar dibutuhkan konversi massa dan jumlah molekul ke dalam bentuk mol. Hubungan antara massa dan mol ditunjukkan oleh persamaan di bawah ini.
Konsep Mol
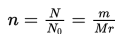
dengan,
No = bilangan Avogadro = 6,02x1023 molekul/mol
Mr = massa molekul relatif
No = bilangan Avogadro = 6,02x1023 molekul/mol
Mr = massa molekul relatif
Berikut ini merupakan konversi suhu dan tekanan ke dalam sistem SI :
0o = 273 K;
1 atm = 1,01x105 N/m2=1,01x105 Pa.
0o = 273 K;
1 atm = 1,01x105 N/m2=1,01x105 Pa.
S1
Gas dalam ruang tertutup memiliki suhu 42o C, tekanan 7 atm, dan volume 8 liter. Apabila gas tersebut dipanaskan sampai suhunya menjadi 87o C dan tekanan naik sebesar 1 atm, maka volume gas menjadi ....
S2
16 gr Oksigen (Mr = 32 gr/mol) berada pada tekanan 1 atm dan suhu 27o C, maka volume oksigen di dalam tabung tersebut adalah ....
S3
Jika suatu gas ideal bervolume V1 dimampatkan secara isotermik (T1=T2) sampai volumenya menjadi setengah dari mula-mula (0,5 V1), maka ….
S4
Suatu gas ideal mula-mula menempati ruang yang volumenya V dan tekanan P pada suhu T. Jika suhu gas menjadi 1,25 T dan volumenya menjadi 0,75 V, maka tekanannya menjadi….
S5
Volume tabung B 2 kali volume tabung A (VB = 2VA). Kemudian, kedua tabung tersebut diisi dengan gas ideal dengan jumlah mol di dalam tabung A (nA) dan B (nB) berturut-turut N dan 3N. Bila gas dalam tabung A bersuhu 300 K maka suhu gas dalam tabung B adalah….
S6
Sebuah tabung yang volumenya V1 liter mempunyai lubang yang memungkinkan udara dapat keluar. Mula-mula suhu udara dalam tabung 127o C (T1 = 127o C). Jika kemudian tabung didinginkan hingga suhunya mencapai 27o C (T2 = 27o C), maka perbandingan antara volume gas yang keluar dari tabung dan volume awalnya adalah….
S7
Di dalam tabung pengisi ban terdapat unsur nitrogen (N2) dengan massa jenis 1,25 kg/m3, suhu 27o C dan tekanan 1 atm. Kemudian gas tersebut dipompakan ke dalam ban mobil yang bertekanan 0,97 x 105 Pa sehingga suhunya naik menjadi 42o C. Massa jenis gas nitrogen di dalam ban tersebut adalah ....
S8
Sebanyak 20 mol gas monoatomik berada dalam tabung tertutup yang bervolume 2 m3 dengan energi kinetik molekul rata-rata (Ek) sebesar 2x1020 Joule (bilangan Avogadro 6,02 × 1023 molekul/mol). Tekanan gas dalam tabung adalah ....
S9
Di dalam sebuah tangki yang bervolume 50 dm3 terdapat gas oksigen dengan suhu 27o C dan tekanan 135 atm. Massa gas oksigen di dalam tangki tersebut adalah ….
S10
Sebuah bejana yang bervolume 1 m3 memiliki tekanan uap air sebesar 3x104 Pa. Kemudian, bejana tersebut diletakkan dalam ruangan bersuhu 27o C. Banyaknya uap air yang terdapat dalam bejana pada kondisi tersebut adalah ....
