Contoh Soal Menentukan oksidator dan reduktor
Contoh Soal Menentukan oksidator dan reduktor - Pada topik sebelumnya, kita telah mempelajari tentang reaksi oksidasi dan reduksi dan penentuan bilangan oksidasi. Dalam topik ini, kalian akan mempelajari tentang oksidator dan reduktor, khususnya bagaimana cara menentukan oksidator dan reduktor.
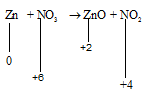
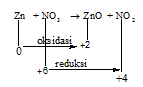
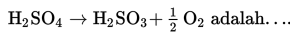


Mari kita ingat kembali topik reaksi oksidasi dan reduksi sebelum masuk ke topik oksidator dan reduktor.
REDOKS
1.Reaksi Reduksi dan Oksidasi (REDOKS)
Reaksi reduksi dan oksidasi, dapat dipahami dari 3 aspek, yaitu:
a. Konsep Oksigen
- Oksidasi : reaksi pengikatan oksigen oleh suatu atom.
Misalnya: 2 Mg + O2 → 2MgO
- Reduksi : reaksi pelepasan oksigen dalam suatu senyawa.
- Misalnya: 2Na2O →2Na + O2.
b. Konsep Elektron
- Oksidasi : reaksi pelepasan elektron.
Misalnya: 2Cl- →Cl2 + 2e.
- Reduksi : reaksi pengikatan elektron.
Misalnya: Na+ + e → Na.
c. Konsep Bilangan Oksidasi
- Oksidasi : reaksi peningkatan bilangan oksidasi.
- Reduksi : reaksi penurunan bilangan oksidasi.
Misalnya:
Reaksi reduksi dan oksidasi, dapat dipahami dari 3 aspek, yaitu:
a. Konsep Oksigen
- Oksidasi : reaksi pengikatan oksigen oleh suatu atom.
Misalnya: 2 Mg + O2 → 2MgO
- Reduksi : reaksi pelepasan oksigen dalam suatu senyawa.
- Misalnya: 2Na2O →2Na + O2.
b. Konsep Elektron
- Oksidasi : reaksi pelepasan elektron.
Misalnya: 2Cl- →Cl2 + 2e.
- Reduksi : reaksi pengikatan elektron.
Misalnya: Na+ + e → Na.
c. Konsep Bilangan Oksidasi
- Oksidasi : reaksi peningkatan bilangan oksidasi.
- Reduksi : reaksi penurunan bilangan oksidasi.
Misalnya:

2. Oksidator dan Reduktor
Oksidator (pengoksidasi) adalah senyawa yang mengoksidasi senyawa lain. Oksidator sendiri mengalami reaksi reduksi. Sedangkan reduktor (pereduksi) adalah kebalikannya, yaitu zat yang mereduksi senyawa lain. Reduktor mengalami reaksi oksidasi.
Oksidator (pengoksidasi) adalah senyawa yang mengoksidasi senyawa lain. Oksidator sendiri mengalami reaksi reduksi. Sedangkan reduktor (pereduksi) adalah kebalikannya, yaitu zat yang mereduksi senyawa lain. Reduktor mengalami reaksi oksidasi.
Untuk lebih jelasnya, mari perhatikan contoh berikut:
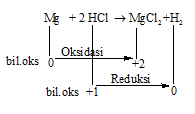
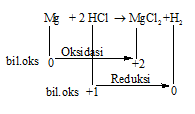
Pada reaksi Mg + 2 HCl → MgCl2 +H2
Pada reaksi Mg + 2 HCl → MgCl2 +H2

Oksidator: HCl
Reduktor: Mg
Reduktor: Mg
3.Cara Menentukan Oksidator dan Reduktor
Cara menentukan oksidator dan reduktor, dapat dilakukan dengan tahapan berikut.
a. Tuliskan kerangka reaksinya
b. Tentukan zat yang mengalami perubahan bilangan oksidasi (biasanya selain O dan H)
c. Hitung perubahan bilangan oksidasi dari zat-zat tersebut
d. Tentukan jenis reaksinya, Oksidasi (mengalami kenaikan bilangan oksidasi) atau reduksi (mengalami penurunan bilangan oksidasi)
e. Tentukan oksidator dan reduktornya.
Cara menentukan oksidator dan reduktor, dapat dilakukan dengan tahapan berikut.
a. Tuliskan kerangka reaksinya
b. Tentukan zat yang mengalami perubahan bilangan oksidasi (biasanya selain O dan H)
c. Hitung perubahan bilangan oksidasi dari zat-zat tersebut
d. Tentukan jenis reaksinya, Oksidasi (mengalami kenaikan bilangan oksidasi) atau reduksi (mengalami penurunan bilangan oksidasi)
e. Tentukan oksidator dan reduktornya.
Untuk lebih memperjelas materi ini, mari kita perhatikan contoh-contoh berikut.
Contoh 1
Tentukan oksidator dan reduktor pada reaksi Zn + NO3 → ZnO + NO2
Tahapannya:
~Tulis reaksinya : Zn + NO3 → ZnO + NO2
~Zat yang mengalami perubahan bilangan oksidasi adalah Zn dan N
~Hitung perubahan bilangan oksidasinya
Contoh 1
Tentukan oksidator dan reduktor pada reaksi Zn + NO3 → ZnO + NO2
Tahapannya:
~Tulis reaksinya : Zn + NO3 → ZnO + NO2
~Zat yang mengalami perubahan bilangan oksidasi adalah Zn dan N
~Hitung perubahan bilangan oksidasinya
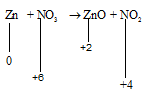
~Jenis reaksinya
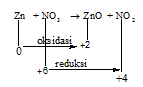
~Oksidator: NO3 (mengalami reaksi reduksi) dan reduktor, Zn (mengalami reaksi oksidasi).
S1
Pernyataan yang benar tentang oksidator adalah....
S2
Saat terjadi perubahan MnO menjadi MnO2, bilangan oksidasi Mn adalah....
S3
Pada reaksi pembentukan NaCl, reduktornya adalah....
S4
Pernyataan yang benar untuk reaksi
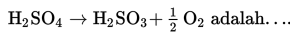
S5
Pada reaksi NaClO2 + 2 Mg → NaCl + 2 MgO, senyawa yang bertindak sebagai reduktor adalah....
S6
Reaksi komporporsionasi adalah reaksi dimana hasil reduksi dan oksidasi merupakan zat yang sama. Salah satu reaksi tersebut adalah H2O + NaClO + NaCl → 2NaOH + Cl2. Reduktor dan oksidator pada reaksi tersebut berturut-turut adalah....
S7
Berikut disajikan beberapa reaksi.

Menurut konsep bilangan oksidasi, reaksi yang memiliki oksidator dan reduktor adalah....
S8
Pengertian reduktor menurut konsep elektron adalah....
S9
Perhatikan reaksi berikut.
LiCl + Na → NaCl + Li
Pada reaksi tersebut, atom yang mengalami perubahan bilangan oksidasi adalah....
LiCl + Na → NaCl + Li
Pada reaksi tersebut, atom yang mengalami perubahan bilangan oksidasi adalah....
S10

Berdasarkan reaksi di atas, reduktornya adalah....
